以前の記事「UPCはProblem Solution Approachを捨てました」では欧州特許庁(EPO)における進歩性判断と同様に統一特許裁判所(UPC)における進歩性判断の際にも「合理的な成功の期待(Reasonable expectation of success)」が検討事項となることを説明しました(「合理的な成功の期待」って何?という方は過去の記事「UPCでは医薬・バイオテクノロジー関連の発明の進歩性が否定されやすいです」をご参照ください)。
しかしこの「合理的な成功の期待(Reasonable expectation of success)」のハードルが欧州特許庁と統一特許裁判所とで同じとは限りません。
今回は同一の証拠に基づいて同一のクレームの進歩性が争われたにも関わらず、「合理的な成功の期待」の有無で判断が分かれた欧州特許庁の審決T 0136/24そして統一特許裁判所ミュンヘン地方部の判決UPC_CFI_146/2024 et al.を紹介します。
背景
本件特許クレーム1
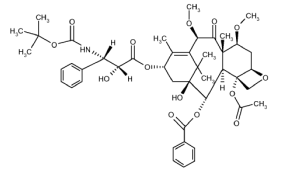
式1の化合物であって
以前にドセタキセルベースのレジメンで治療されたことがあり、かつ、前記治療中または治療後に進行した前立腺がんを有する、去勢抵抗性転移性前立腺がんの患者におけるプレドニゾンまたはプレドニゾロンと組み合わせた前立腺がんの治療に用いられる化合物。
明細書に開示されたデータ
式1の化合部およびプレドニゾンの投与を受けた患者が、ミトキサントロンおよびプレドニゾンの投与を受けた患者よりも、全生存期間が長い。
先行技術文献 第3フェーズ「TROPIC」臨床試験プロトコル
以前にドセタキセルベースのレジメンで治療されたことがあり、かつ、前記治療中または治療後に進行した前立腺がんを有する、去勢抵抗性転移性前立腺がんの患者に式1の化合物およびプレドニゾンを投与したことが開示されていた。ただし式1の化合部およびプレドニゾンの投与が実際に全生存期間を延長させたことを示唆するデータは存在していなかった。
欧州特許庁 審判部の判断 T 0136/24
「臨床試験の承認は、得られる知見の妥当性という観点から期待される利益と、参加者に対する予見可能なリスクとの評価に依存するものであり、これは必ずしも肯定的な結果が期待されること(expected positive outcome)を意味するものではなく、試験対象の治験薬の開発プログラムに関する科学的助言を意味するものでもない。したがって、臨床試験の承認は、必ずしも肯定的な結果が期待されることを意味するものではない。」(審決の理由7.14.3参照)
「文献D4およびD26の開示内容の分析(上記6.12.6項参照)からわかるように、前臨床段階のデータはまばらで不完全なものであった。」(審決の理由7.15.2参照)
「当業者は、関連する患者群において有効な治療を達成できるとの合理的な成功の期待を有しておらず、せいぜい成功への希望を抱いていたにすぎなかった。」(審決の理由7.35.4参照)。
統一特許裁判所 ミュンヘン地方部の判断 UPC_CFI_146/2024 et al.
「TROPIC試験が承認され、優先日の時点で中止されることなく3年間進行していたという事実から導き出せるのは、少なくともこの試験のスポンサーは、開始時においても、また優先日までのいかなる時点においても、この試験を期待外れ(失敗)とは見なしていなかったということである。試験終了の6ヶ月前において、臨床試験では試験計画に従って定期的に利益とリスクの観点から中間結果を評価しなければならないことを知っており、かつ、否定的な事象が発生または公表されていないことに気づいている当業者は、当該患者グループの治療におけるカバジタキセルとプレドニゾンの併用について、合理的な成功の期待を抱いていたはずである。」(判決文41ページ参照)
解説
上述のように欧州特許庁は、治療効果を示すデータが不完全であることを理由に「合理的な成功の期待」を否定しました。つまり欧州特許庁において「合理的な成功の期待」が認められ、そして進歩性を否定するには、治療効果を示す証拠が先行技術から導出可能であることが求められることがわかります。
一方で統一特許裁判所は治療効果を示すデータが不完全であることは認めつつも、第3フェーズ臨床試験の存在自体が「合理的な成功の期待」の根拠となり得るとしています。つまり今回の判決を参照する限りは、統一特許裁判所で採用される「合理的な成功への期待」のハードルは、欧州特許庁のそれよりも低く、進歩性が否定されやすいことが示されます。